| 
1. Inleiding
 |
Elke vergister
heeft al te maken gehad met te hoge uitstoot van H2S
in het biogas. De aanwezigheid van H2S in het biogas
leidt niet alleen tot problemen op de wkk's (gaten in
de zuigers, breken van de klepvoeten, vermogenverlies...), |
maar heeft ook belangrijke
gevolgen op de conversieefficiëntie van de organische
stof in methaan (zie verder in dit artikel). Overmaat aan
oplosbare sulfiden (lees H2S) in de vergister kunnen evenwel
een vergiftiging veroorzaken van de biologische fauna.
- Waar komt deze H2S vandaan?
- Hoe kan men dit verhelpen?
- Welke gevolgen heeft de aanwezigheid
van sulfiden op het biogaspotentieel van de grondstoffen?
2. Herkomst van de H2S productie
H2S wordt geproduceert vanuit
elke vorm van geoxideert zwavel die aanwezig is in de vergister.
Sulfatoreducerende
bacteriën zetten deze vormen zwavel om in sulfiden
(S--) zodat de zwavel dan op zijn laagste oxidatiegetal staat.
Op het gebied van voeding
zal men hoofdzakelijk geoxideerd zwavel terugvinden in:
-
sufaatbevattende grondstoffen waarin
de sulfaten door een industrieel proces werden ingevoerd
(de meeste vinassen en producten die op ionenwisselars
werden behandeld)
-
natieve organische stoffen: hier komt
de zwavel quasi exclusief van de twee zwavelhoudende aminozuren:
methionine en cysteine. Aminozuren zijn de basisblokken
van eiwitten. b.v. een tarwegluten zal steeds meer zwavel
aanbrengen dan een sojaeiwit omdat het rijker is aan deze
twee aminozuren.
-
Opgelet, bruuske pieken H2S kunnen
van een dag tot een ander voorkomen wanneer de atomische
zwavel (de geelkleurige poeder die u op de kijkruiten
ziet van de vergister, oxidatiegetal=0) dat neergeslaan
is op de rand van de vergister inneens loskomt en in de
vergister valt. Deze zwavel, die op het oxidatieniveau
0 staat, wordt dan zeer snel omgezet in sulfiden (en dus
H2S) door de sulfatoreducerende bacteriën.
Voor de SRB's (sulfatoreducerende
bacteriën) speelt het geoxideerd zwavel de rol van electronen
acceptor (identieke rol dat zuurstof speelt bij aërobe
organismen) tijdens de oxidatie van organische stof om energie
te produceren.
De biochemische aspecten
van de energiestofwisseling van srb's is buiten het bereik
van dit artikel. Onthou gewoon het volgende:
Elke keer dat er geoxideert
zwavel in de vergister aanwezig is zullen de SRB's deze prioritair
omzetten in H2S voor de neus van de methanogenen. De SBR's
zullen al het acetaat omzetten naar CO2 dat mogelijk gemaakt
wordt door het reduceren van de aanwezige zwavel! Acetaat
is het voedsel voor de methanogenen (dat wordt omgezet naar
50% CO2 en 50% CH4). Dit is dus werkelijk een voedsel verspilling
voor methaanproductie. Weg is weg! Resultaat: veel CO2 en
weinig CH4 in het biogas.
Ook wanneer een vergister
voortdurend met een zwavelarme grondstoffen wordt gevoed kunnen
bruuske pieken in H2S-gehalte worden waargenomen. Waarom?
Laat ons even een illustratie geven van de val van klonten
zwavel in de vergister. Neem een vergister van 4000m3 die
640m3/u biogas produceert. En fijne 1mm laag gele zwavel op
het bovenste gedeelte van de vergister vertegenwoordigt 140
kg zwavel. Indien één honderdste van deze laag
in de vergister valt (1.4kg zwavel) geeft dit een verhoging
van 500ppm H2S in het biogas gedurende 24 dagen (of 1000ppm
gedurende 12 dagen, of 2000ppm gedurende 6 dagen enz...)!!
3. Physiologische effecten van H2S
op de mens
H2S dringt voornamelijk het
lichaam binnen via de longen. De biochemische mechanismen
van de sulfidetoxiciteit valt buiten de scope van dit artikel.
Daarom geven wij hier slechts een samenvatting van de physiologische
effecten op enkele H2S concentraties:
| ppm H2S |
symptomen op de mens |
| 0.02 - 0.13 |
Rotte eieren geur |
| 50 |
slijmvlies irritatie (ogen en ademhalingswegen) |
| 100 |
keelirritatie |
| 100 - 150 |
bewustloosheid |
| 250 - 500 |
hoofdpijn, cyanose, longoedeem |
| 500 - 1000 |
Ataxie, misselijkheid, aantasting van de mentale vermogens |
| >1000 |
Apnea, verlamming van het zenuwstelsel en dood in enkele
minuten |
| >5000 |
dood |
OPGELET, vanaf 100ppm ruikt
men niets meer (geen rotte eierengeur meer). Dan wordt de
expositie echt gevaarlijk. |

4. Invloed van de pH van het digestaat
op het H2S-gehalte in het biogas
H2S is een zwak zuur. Volgens
het pH gaat H2S zich ontbinden naar volgende species:
H2S + H2O <=> HS-
+ H3O+ (pKa1 = 7.00)
HS- + H2O <=> S--
+ H3O+ (pKa2 = 12.92)
Van deze drie species zwavel
(H2S, HS- en S--) is H2S de enige die gasvormig is. Omdat
de pKa1 dicht bij de pH-waarden die in de vergister heersen,
zal het biogas H2S-gehalte sterk varieren voor kleine pH wijzigingen.
Met andere woorden:
- Minder H2S in het biogas wanneer de pH
licht stijgt
- Meer H2S in het biogas wanneer de pH licht
daalt
Dit wordt zichtbaar gemaakt
in de volgende figuur:
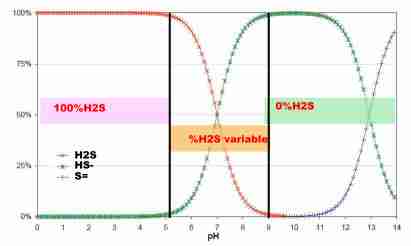
Op zure pH, links gedeelte
van de grafiek, zal al de gereduceerde zwavel zich bevinden
onder de vorm van H2S. Dus Hoog gehalte aan H2S in het biogas,
schadelijk voor de wkk's, maar detoxificatie van de vergister.
Op hogere pH waarden, rechts
gedeelte van de grafiek, gaat de gereduceerde zwavel zich
onder bisulfide (HS-) en sulfide (S--) vorm bevinden. Dus
minder H2S in het biogas maar verhoging van het vergiftigingsrisico
en daling van de conversieefficientie van organische stof
naar methaan.
5.
Effect van H2S op de WKK's
Tijdens de combustie, wordt
H2S geoxideerd in S2 en SO4--. Dit heeft twee gevolgen op
de gezondheid van de motor:
 |
- SO4-- vormt zwavelzuur
(=sterk zuur) dat gaten gaat boren in de Aluminium
zuigers.
- het atomische zwavel
S2 (=gele poeder) bezinkt op de uitlaatkleppen. Eerst
zal de compressie verminderen (vermogensverlies) door
de slechte sluiting van de kleppen. Eindelijk breken
de klepvoeten.
|
6.
Toxische effecten op de bacteriële fauna
H2S is niet enkel toxisch
voor de bacteriële fauna van de vergister, het is ook
het symptoom dat aanduidt dat een hoeveelheid acetaat (azijnzuur)
ontnomen is van de methanogenen door de SRB's. De methanogenen
worden op deze manier van hun voedsel beroofd. Idem voor
wat de waterstof betreft (H2 is het tweede voedsel van de
methanogenen om methaan te produceren). Gevolg: methaangehalte
van het biogas daalt.
Een maal dat de geoxideerde
zwavel volledig is omgezet kan de methanogene fauna weer
het acetaat verwerken. Dit gebeurt echter nooit wanneer
men continu sulfaatrijke grondstoffen blijft voeden.
Noteer toch dat zelfs bij
een zwavelarme voeding in vergisters waar men m.b.v. lucht
ontzwavelt toch nog pieken H2S kunnen voorkomen doordat:
- men te veel lucht blaast.
De gele atomische zwavel wordt dan verder geoxideerd naar
sulfaten (SO4-- die oplosbaar zijn in water). De sulfaten
lopen dan lekker weer in de vergister en de SRB-cyclus herbegint.
- temperatuurschommelingen
die de gele zwavel verkruimelen. De zwavel valt in de vergister
en wordt weer omgezet naar H2S door de SRB's
7. Gevolgen van H2Sproductie
op het biogas potentieel van de organische stof
De aanwezigheid van geoxideerde
zwavel in de vergister (waarvan het H2S een symptoom is)
mag niet worden onderschat. Zoals eerder gezegd zullen de
SRB's al het acetaat omzetten naar CO2 dat mogelijk wordt
gemaakt door de reductie van de zwavel. Ondertussen zit
men organische stof te verspillen die dus nooit methaan
zal produceren.
Laat ons even berekenen
hoeveel men verspilt aan de hand van een eenvoudig voorbeelt:
TO BE CONTINUED
|

8. Curatieve actiemiddelen
Er bestaan verschillende
curatieve actiemiddelen om het H2S gehalte te onderdrukken
in het biogas. Elke van deze heeft een antal voor- en nadelen:
- lucht inblazen in de hemel
van de vergister zodat de sulfo-oxyderende bacteriën
(Thiobacillus spp.) de H2S omzetten naar elementair zwavel
(geel). Opgelet, te veel zuurstof zal de oxydatie voortzetten
tot zwavelzuur dat in de vergister zal lopen!!
- injectie van ijzerchlorideIII
in de vergister
- incorporatie van ijzeroxide
of ijzerhydroxide in de vergister
- gaswasser met ijzerchlorideIII
voor de injectie in de WKK's
- gaswasser voor de WKK's
met ijzeroxide of ijzerhydroxide.
- actievekoolfilters voor
de WKK's
Voor nutritionisten als wij
blijft de vuistregel:
- gooi niets in de vergister
dat de evenwichten van de bacteriële fauna kan verstoren.
- gebruik dus liever de
gaswassing of lucht inblazing in de hemel van de vergister
Toch nog een commentaar over
ijzerchloride. Ijzerchloride gaat reageren met H2S om zoutzuur
en ijzersulfide te produceren. Al zou in theorie deze reactie
niet mogelijk zijn (een zwak zuur kan een sterk zuur uit zijn
zout niet extraheren) gaat deze toch door in de praktijk omdat
men een bezinksel produceert (ijzersulfide) en een gas vormt
(zoutzuur). Resultaat hiervan is het injecteren van een sterk
zuur (zoutzuur) in de WKK's wat uit ten boze is voor de zuigers.
Alleen wordt er geen monitoring gedaan van het zoutzuurgehalte
van het biogas. Men verbergt dus de symptomen.
Dus, liever ijzeroxide of
ijzerhydroxide dan ijzerchloride. Deze twee eertse zetten
evenwel H2S om in ijzersilfide maar produceren water als nevenproduct
ipv een sterkzuur.
9. Preventieve actiemiddelen:
voeding van de vergister
9.1 Rationele zwavel voeding
Om geen problemen tegen te
komen met H2S is het van groot belang rekening te houden met
het zwavelgehalte van de grondstoffen wanneer men een rantsoen
berekent.
Met andere woorden, het is
perfect mogelijk sommige ingredienten te gebruiken die tamelijk
wat zwavel inhouden (gluten, raapzaad, vinassen enz...), maar
men moet rekening houden met de totale hoeveelheid zwavel
die men dagelijks voedt.
Hieronder een aantal grondstoffen
met dalende zwavelgehalte op droge stof (!!! op verse stof
telt niet. voor een vergister moet men steeds rantsoenen opstellen
op droge stof!!!)
minerale
sulfaten > glutens (= eiwitten van graangewassen) >
melassen > alguen > depotassificatie vinassen > haar
en pluimen > eipoeder> vismelen > maïs weekwater
> diermelen > gistcellen > maniok > soja schilfers
en schroot > vlasschilfers > CCM > bietpulp >
sojabonen > eidooiers > grondnootschroot > melk en
kaas > raapzaadschroot > kaasweipoeder > tarwe >
graankaf > gerst > sojapeulen > brood > korrelmaïs
> pluimveemest > bietenloof > raapzaadresten (screenings)
> KuilMaïs > suikerbiet > aardappel
> rijst > gedeproteïneerde kaaswei.
Deze lijst is ver van alomvattend
maar zal u in één oogslag sommige bijproducten
te situeren waarvoor u oplettend dient te blijven wanneer
u uw rantsoen opstelt.
Wij blijven uiteraard ter
uw beschikking om u bij de opmaak van rantsoenen bij te wonen.
9.2 Gebruik van de Hydrolysetank
Wanneer de keuze van de grondstoffen
niet mogelijk is, is het van belang de hydrolyse tank in gebruik
te nemen voor de zwavelrijke grondstoffen. Op laag pH, bestaan
sulfiden hoofdzakelijk in de vorm van H2S. Deze worden samen
met de CO2 verwijderd uit de hydrolyse tank. Ontzwavelen van
zwavel-rijke materialen m.b.v. de hydrolyse tank is een goedkope
methode. Het is echter noodzakelijk te beschikken over voldoende
snel afbreekbare grondstoffen (rijk aan suikers en zetmeel)
om de pH van de tank laag te houden (onder pH 5,6 door hoge
vrije vetzurenproductie). Als men niet in staat is de pH laag
te houden zal de metaanproductie in de hydrolysetank op stand
komen met de samenhangende efficiëntieverlies.
|

