| 
1. Introduction
 |
Chaque biométhaniseur
a déjà été confronté
à des taux élévés d'H2S
dans le biogaz. La présence d'H2S ne cause pas
seulement des problèmes sur les moteurs de cogénération
(trouage des pistons et casses des soupapes d'échappement,
perte de puissance...), |
mais implique des pertes
d'efficience de la conversion d'aliments en méthane
(voir plus loin dans cet article) et peut également
provoquer l'intoxication de la faune du digesteur.
- D'où vient l'H2S?
- Comment peut-on y remComment peut-on y reméédier?
- quelles sont les implications de
la présence d'H2S sur le potentiel biogaz de la matière
organique?
2. Origine de la production d'H2S
L'H2S est produit à
partir de toute forme de soufre oxydé présent
dans le digesteur. Ce sont les bactéries
sufato-réductrices (BSR) qui sont à l'origine
de la production d'H2S.
Du point de vue de l'alimentation,
les formes oxydées de soufre se trouvent dans:
-
les matières minérales
sous forme de sulfates (p.ex. dans de nombreuses vinasses
issues de la régénération des échangeurs
d'ions à l'acide sulfurique)
-
Les matières organiques: quasi
exclusivement 2 acides aminés (cystéine
et méthionine) qui sont deux "briques de base"
des protéines
-
Attention, des poussées de H2S
sont possibles lorsque du soufre déposé
sur le béton et la charpente du digesteur retombe
par blocs dans le digestat. Dans ce cas, on assiste à
des variations fortes de la teneur en H2S dans le biogaz
d'un jour à l'autre.
Pour les BSR, le soufre oxydé
joue le rôle d'accepteur d'électrons lors de
l'oxydation de la matière organique pour produire l'énergie
dont la bactérie a besoin. Les considérations
biochimiques du métabolisme énergétique
des BSRs sort du cadre de ce dossier. Aussi, retenez simplement
que chaque fois qu'il y a présence de soufre oxydé
dans un digesteur, les BSR auront priorité absolue
sur les bactéries méthanogènes quant-à
l'utilisation l'acide acétique. Il en résultera
une production de biogaz appauvri en méthane et riche
en H2S.
Afin d'illustrer le résultat
de la chute de soufre des parois du digesteur dans le digestat,
nous faisons un calcul rapide des conséquences: dans
un digesteur de 4000m3 qui produit 640m3 de biogaz par heure,
une couche de 1mm de soufre atomique sur la paroi latérale
de béton représente environ 140 kg de souffre.
Un centième de cette quantité (c-à-d
1.4 kg de soufre) qui retomberait dans le digestat expliquera
un taux de H2S accru de 500ppm dans le biogaz pendant 24 jours!!
3. Effets physiologiques sur l'être
humain
L'H2S pénètre
essentiellement dans l'organisme par voie pulmonaire. Les
mécanismes biochimiques de la toxicité des sulfures
sort du cadre de cet article. Nous nous bornerons donc à
résumer les effets physiologiques de différentes
concentrations en H2S.
| ppm H2S |
symptômes chez l'homme |
| 0.02 - 0.13 |
perception olfactive (odeur d'oeufs pourris |
| 50 |
irritation des muqueuses (yeux, voies respiratoires |
| 100 |
irritation de la gorge |
| 100 - 150 |
perte de conscience |
| 250 - 500 |
mal de tête, cyanose, oedème pulmonaire |
| 500 - 1000 |
Ataxie, nausées, facultés intellectuelles
perturbées |
| >1000 |
Apnée, paralysie du système nerveux et
mort en quelques minutes |
| >5000 |
mort immédiate |
ATTENTION: à partir
de 100ppm on ne sent plus l'odeur d'oeufs pourris alors que
les concentrations deviennent réellement dangereuses. |

4. Effets du pH du digestat sur
le H2S dans le biogaz
Le H2S est un acide faible.
Selon le pH il se décompose dans l'eau:
H2S + H2O <=> HS-
+ H3O+ (pKa1 = 7.00)
HS- + H2O <=> S--
+ H3O+ (pKa2 = 12.92)
De ces trois espèces,
seul le H2S est une forme gazeuse et se retrouve donc dans
le biogaz. Or comme le pKa1 est proche du pH qui règne
dans un digesteur, on assistera à de très fortes
variations de la concentration de H2S dans le biogaz pour
de très faibles variations de pH des digestats.
En d'autres mots:
- il y aura moins de H2S dans le biogaz
lorsque le pH monte légèrement
- il y aura moins de H2S dans le biogaz
lorsque le pH baisse légèrement
Ceci est bien résumé
dans le graphique suivant:
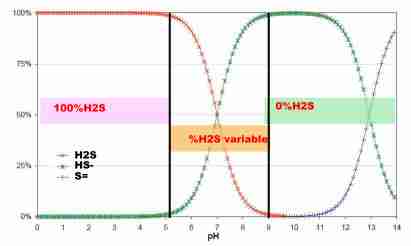
Aux pH acides, sur la portion
gauche du graphique, tout le soufre réduit se trouve
sous forme de H2S et passe donc dans le biogaz. Le digestat
se détoxifie mais le biogaz est nocif pour les moteurs.
Aux pH plus élevés,
tout le soufre résduit se trouve sous forme de bi-sulfures
puis de sulfures qui restent en solution (peu de H2S dans
le biogaz mais beaucoup de soufre dans le digesteur avec risque
d'intoxication H2S et perte d'efficacité de la conversion
de la matière organique en méthane).
5. Effets du H2S sur les moteurs
de cogénération
Lors de la combustion, le
H2S s'oxyde en soufre atomique et en sulfate. Ceci a deux
implications sur l'usure et les casses moteur:
 |
- Les sulfates forment
de l'acide sulfurique qui attaque les pistons en aluminium
et finit par les trouer.
- le soufre atomique
précipite sur les soupapes. diminue dans un
premier temps la compression et finit par casser les
pieds de soupapes.
|
6. Effets toxiques
sur la faune bactérienne
Le H2S n'est pas extrêmement
toxique pour la faune méthanogène mais il
permet surtout aux BSR d'être compétitive par
rapport aux bactéries méthanogènes
quant à l'utilisation de l'acide acétique.
Privant la faune méthanogène de son substrat
principal, il en va de même pour l'oxydation de l'hydrogène.
Il en résulte une diminution de la qualité
du biogaz.
Une fois les sulfates consommés
et l'alimentation appauvrie en soufre oxydé, la flore
méthanogène peut reprendre sa production de
méthane rapidement.
Il faut noter que même
lorsque l'alimentation est pauvre en soufre, dans les installations
qui désulfurisent le biogaz au niveau du digesteur
par insuflation d'oxygène, il peut apparaître
des sauts de H2S dans le biogaz. ceci provient de essentiellement
de:
- insuflation trop importante
d'oxygène par laquelle le soufre atomique (poudre
jaune) s'oxyde en sulfate soluble qui coulera dans le digestat
et réactivera les BSR.
- variations de températures
dans le digesteur qui provoquent l'effritement du soufre
atomique qui retombe par blocs dans le digesteur.
7. Effets du H2S
sur le potentiel biogaz de la matière organique
La présence de soufre
oxydé dans le digesteur (dont le syptôme est
une taux élevé de H2S dans le biogaz) ne doit
pas être sous-estimée. En effet, les BSR consomment
l'acide acétique et l'hydrogène autant qu'il
est possible, c'est-à-dire tant qu'il y a des sulfates
à réduire en H2S. Pendant ce temps, les méthanogènes
sont privées d'aliment pour former du méthane.
Le H2S n'est que modérément
toxique pour les bactéries méthanogènes.
L'effet inhibant pour les méthanogènes est
surtout un privation de leurs substrats: l'acétate
et l'hydrogène. En effet, la voie métabolique
de la sulfato-réduction est énergétiquement
plus rentable que l'oxydation de l'acétate en CO2
et en méthane. Les BSR prennent donc le dessus sur
les méthanogènes.
Pour comprendre pourquoi
le rendement de la matière organique est diminué
par la présence de soufre oxydé, il faut mettre
les deux voies métaboliques d'oxydation de l'acétate
(sulfato-réduction et méthanisation) côte
à côte:
méthanisation:
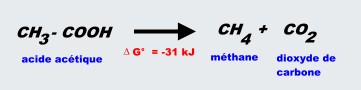
sulfato-réduction:
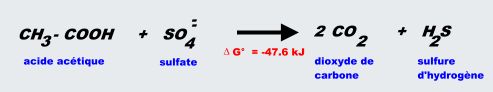
Pour le biométhaniseur,
il est clair que l'acétate ne produit pas de méthane
lorsqu'il est oxydé par sulfatoréduction puisqu'il
ne se transforme que en CO2. Une partie de l'alimentation
du digesteur est donc gaspillée. Le symptome de ce
gaspillage est la forte présence de H2S dans le biogaz.
Nous allons tenter
de quantifier les pertes d'efficience de la conversion de
la matière organique en méthane lors de la
biométhanisation et ceci en fonction du H2S mesuré
dans le biogaz.
Comme scientifiques nutritionnistes,
nous ne procédons pas par la mesure de H2S dans le
biogaz mais bien dans l'ensemble de la ration journalière.
Pour le biométhaniseur qui dispose de la mesure de
la concentration en H2S dans le biogaz (capteurs à
l'entrée des moteurs), ce petit calcul est plus évocateur.
Ici, afin de ne pas faire
de lourdes erreurs, il faut porter une attention extrême
aux unités utilisées:
- les capteurs H2S donnent
la concentration en ppm (V/V), c'est-à-dire en ml
de H2S/m3 de biogaz et non en g/m3 ou en g/tonne.
- Bien que ce ne soit pas
entièrement exact, nous considérerons que
2/3 du H2S total produit reste dans le digestat et que donc
1/3 se retrouve dans le biogaz (ces proportions dépendent
fortement du pH du digesteur).
- Afin de ne pas compliquer
inutilement les calculs, admettons un aliment unique produisant
150Nm3/tonne. Nous ferons varier sa teneur en H2S au cours
de l'exercice.
CAS 1 biogaz à 300ppm
H2S:
(300/1000)/22.4 = 0.0134
moles/m3 dans le gaz
avec 1 tonne d'aliment,
on produit 150m3 de biogaz, donc 0.0134*150=2.0089 moles
H2S biogaz par tonne d'aliment
2.0089/0.33 = 6.0877 moles
H2S total produit par tonne d'aliment.
6.0877*32/34 = 5.73 g S/tonne
d'aliment = 5.73 mg/kg d'aliment
Maintenant, quelle est
la perte en CH4:
on a 6.0877 moles de H2S
produit par tonne d'aliment. Ceci à donc convertit
6.0877 moles d'acétate en CO2, c'est à dire
6.0877*60= 365 g d'acétate perdus.
on a perdu 6.0877 moles
de méthane pur = 6.0877*22.4 = 136 litres de méthane
pur = 272 Nlitres de biogaz.
Perte d'efficience : 0.272/150=
0.2%
CAS 2 biogaz à 800ppm
H2S:
(800/1000)/22.4 = 0.0357
moles/m3 dans le gaz
avec 1 tonne d'aliment,
on produit 150m3 de biogaz, donc 0.0357*150=5.357 moles
H2S biogaz par tonne d'aliment
5.357/0.33 = 16.234 moles
H2S total produit par tonne d'aliment.
16.234*32/34 = 15.279 g
S/tonne d'aliment = 15.279 mg/kg d'aliment
Maintenant, quelle est
la perte en CH4:
on a 16.234 moles de H2S
produit par tonne d'aliment. Ceci à donc convertit
16.234 moles d'acétate en CO2, c'est à dire
16.234*60= 974 g d'acétate perdus.
on a perdi 16.234 moles
de méthane pur = 16.234*22.4 = 363 litres de méthane
pur = 727 Nlitres de biogaz.
Perte d'efficience : 0.727/150=
0.4%
TO BE CONTINUED
|

8. Moyens d'action
curatifs
Il existe plusieurs moyens
d'abbattement du taux de H2S du biogaz. Chacune des méthodes
comporte des avantages et des inconvénients.
- insufflation d'air dans
le ciel du digesteur permettant aux bactéries du genre
Thiobacillus d'oxyder le H2S en soufre élémentaire.
Attention, trop d'oxygène permettra l'oxydation en
acide sulfurique qui recoulera dans le digesteur!!
- injection de chlorure ferrique
dans le digesteur
- incorporation d'oxyde de
fer ou d'hydroxyde de fer dans le digesteur
- lavage du biogaz devant
le moteurs avec du chlorure ferrique
- lavage du biogaz devant
le moteurs avec de l'oxyde de fer ou de l'hydroxyde de fer.
- filtres à charbon
actif avant le moteur
Pour des nutrionnistes comme
nous, il y a une règle d'or:
- n'introduisez aucune
molécule dans votre digesteur qui risquerait de déstabiliser
les équilibres biologiques des faunes bactériennes.
- utilisez préférentiellement
les méthodes de lavage des gaz en aval ou éventuellement
l'insufflation d'air dans le ciel du digesteur.
Encore une chose qui nous
semble être importante au sujet du chlorure de fer et
à laquelle on ne pense pas souvent. Le chlorure de
fer réagit avec l'H2S pour formet du sulfure de fer
et de l'acide chlorhydrique (même si cette réaction
semble théoriquement impossible car un acide faible
ne peut extraire un acide fort de son sel), elle se produit
quand même dans la pratique car le sulfure de ferII
est un précipité et l'acide chlorhydrique est
un gaz qui déplacent l'équilibre de le Chatelier
vers la formation d'acide chlorhydrique! On se retourve donc
avec de l'acide chlorhydrique dans le biogaz injecté
dans les moteurs de cogénération qui troueront
encore mieux les pistons...
Utilizez préferentiellement
l'oxyde de fer ou l'hydroxyde de fer qui transforment le H2S
en sulfure de fer et eau (au lieu d'acide chlorhydrique).
9. Moyens d'action
préventifs: l'alimentation du digesteur
9.1 alimentation rationnelle
en soufre
Afin de ne pas avoir de problèmes
avec l'H2S, il est primordial de tenir compte de la concentration
en soufre dans la ration globale du digesteur.
En d'autres mots, il est
possible d'utiliser certains ingrédients riches en
soufre (gluten, colza, vinasses etc...), mais il faut tenir
compte de leur teneur en soufre lors de leur incorporation
dans la ration.
Les quelques ingrédients
suivants sont classés par richesse en soufre décroissante
(sur matière sèche):
sulfates minéraux
> glutens (proténes de blé) > mélasses
> algues > vinasses de dépotassification >
poils et plumes (abbattoirs) > poudres d'oeufs > farines
de poisson > solubles de maïs > farines de viande
> levure > manioc > tourteau de soja > tourteau
de lin > raffles de maïs > pulpe de betterave >
solubles de maïs > graine de soja > jaune d'oeuf
> tourteau d'arachide > lait et fromages > les tourteaux
de colza > les poudres de lactosérums > le blé
> balles de céréales > orge > cosses
de soja > pain > maïs grain > fiente de volaille
> feuilles et collets de betterave > issues de colza
> ensilage de maïs > betterave
sucrière > pomme de terre > riz > lactosérum
déprotéiné.
Cette liste, loin d'être
exhaustive vous permettra de situer quelques sous-produits
pour lesquels il faut tenir compte de la teneur en soufre
lors de leur introduction dans une ration. Nous restons à
votre dispsition pour vous aider à réaliser
des rations pauvre en soufre.
9.2 Utilisation du tank
à hydrolyse
Lorsque le choix des matières
premières n'est pas possible, il est indispensable
d'utiliser le tank à hydrolyse pour les matières
premières riches en soufre. En effet, à pH faible,
les sulfures se trouvent essentiellement sous forme de H2S
et sont évacués du tank à hydrolyse avec
le CO2. C'est une methodologie peu onéreuse de désulfurer
les matières premières riches en soufre. Il
est cependant indispensable de disposer de suffisamment de
matières premières à dégradation
rapide (riches en sucres et amidons) afin de maintenir le
pH du tank à hydrolyse en dessous de pH 5.6 (production
d'AGV élévée). Dans le cas contraire
il y aura production de méthane dans le tank à
hydrolyse, et donc perte d'efficacité alimentaire.
|

